�G�y���X���]�[���a�`�̃w���v���Y�}����
�@�Â�����m���Ă��銄�ɂ��̑��݂����i�قƂ�Ljӎ�����Ă��Ȃ��̊����ǂ�1 �ɓG�y���X���]�[���a�Ƃ����̂�����܂��B����͂��ē��{�ł��������m�F����ďd�v������Ă����a�C�ł����A�ŋ߂ł͘b��ɂ̂ڂ邱�Ƃ����Ȃ��Ȃ�A���̐Z���ɂ��Ă̒������s���Ă��܂���B�������A�G�y���X���]�[���a�����{�̗{����Ȃ��Ȃ����Ƃ����킯�ł͂���܂���B�ނ���A�Ђ���Ƃ�����F����̔_��Ŏ��̗���тɉe������v���ƂȂ��Ă���\��������܂��B
�@�����ł́A�ŐV�̒m������ɂ����G�y���X���]�[���a�i�w���v���Y�}�a�j�̉���ƁA�����{�؏�ɂ�����g�w���v���Y�}�h �̐Z���ɂ��ďЉ�܂��B
�G�y���X���]�[���a�i�w���v���Y�}�a�j�̗��j
�@���̕a�C�̌����ƂȂ�a���͍̂ŋ߂̌����ŕ��ނ��ύX����A����ɔ����ĕa�����ς��ȂǕ��G�Ȕw�i������܂��B�����ł܂��A�w���v���Y�}�̗��j�ƃw���v���Y�}�a�ɂ��ĊȒP�ɏЉ�����Ǝv���܂��B
�@�̃w���v���Y�}�Ƃ����a���̂ɂ��Ă���܂łɕ��������Ƃ�����l�͂܂����Ȃ��Ǝv���܂����A����͂��ă��P�b�`�A�ڃA�i�v���Y�}�Ȃ̃G�y���X���]�[�����Ƃ��ĕ��ނ���Ă����ۂł��B����炪�����ƂȂ�a�C�̓G�y���X���]�[���a�ƌĂ�Ă��܂����B�G�y���X���]�[�����̍یQ
�͓����̐Ԍ����Ɋ��Ĕ���E���B���邽�߂Ɏ������ł̔|�{���ł����A�������ł̋ۂ̌`�̔�r�A�����̕��@��a�����̈Ⴂ�A�R�������ւ̊��Ȃǂ���ɂ��ĕ��ނ���Ă��܂����B�������A�ߔN�ɂȂ���DNA �����͂����ƁA���͂���炪�}�C�R�v���Y�}�ɑ�����یQ�ł��邱�Ƃ��������܂����B
�@�}�C�R�v���Y�}�ƌ����ƁA�x������[���Ƃ�����ۂ������Ǝv���܂����A���̓}�C�R�v���Y�}�ɂ͔��ɑ����̎킪����A�a�������������ɔ��y�ۂƂ��ē������̂ȂǁA���ɗl�X�ȋێ킪���݂��܂��B���ăG�y���X���]�[���Ƃ���Ă����ێ�͐Ԍ����Ɋ��đ��B����^�C�v�̃}�C�R�v���Y�}�ł���A�����悤�ɐԌ��������������̃}�C�R�v���Y�}�ƍ��킹�āg�w���v���Y�}�h �Ƒ��̂����悤�ɂȂ�A����ɂ����̃w���v���Y�}�̊����ɂ���ċN����a�C���u�w���v���Y�}�a�v�ƌĂ��悤�ɂȂ�܂����i�\1�j�B

�w���v���Y�}�ɂ̓G�y���X���]�[�����Ƃ���Ă����ۂ̂ق��ɁA����L�Ŏ����悤�ȕa�C���N�����A���ăw���o���g�l���Ƃ��ĕ��ނ���Ă����ۂȂǂ��܂܂�܂��B
�@�w���v���Y�}�͎���ِ��������A�Ɋ���������͓݂̂̂ɁA���Ɋ���������̂͋��݂̂Ɋ�������̂����ʂŁA�q�c�W�⌢�A�L�ȂǑ����̓����ɂ��ꂼ�ꊴ������ŗL�̃w���v���Y�}�����݂��܂��B�ێ�ɂ���ĕa�����ɈႢ������܂����A�w���v���Y�}�̊������������͗n�����n���┭�M�A�H�~�s�U�A����x����ɐB��Q�Ȃǂ̉e�����܂��B���������̋}�����ł͐Ԍ����Ɋ���ۂ��ώ@�����悤�ɂȂ�܂��i�ʐ^�j�B�������A�Ǐ�Ƃ��Ă͂قƂ�NJώ@����Ȃ��s���������ɏI��邱�Ƃ������A�܂��f�f�@�����܂蔭�B���Ă��Ȃ����Ƃ������ĕa�C�Ƃ��ĔF������Ȃ��ꍇ�������悤�ł��B
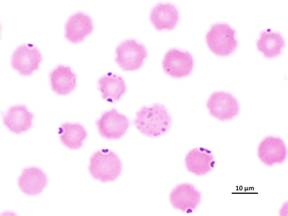
�ʐ^�@�r�̐Ԍ����Ɋ����w���v���Y�}�i��� �q��2011�j
�w���v���Y�}�a
�@�Ɋ�������w���v���Y�}�Ƃ��ẮA�}�C�R�v���Y�}�E�X�C�X�i�ȉ��u�X�C�X�v�j�ƃ}�C�R�v���Y�}�E�p���o���i�ȉ��u�p���o���v�j��2��ނ��m���A�k�Ă�1950�N��ɍŏ��̓w���v���Y�}�a�̔��������ꂽ�̂��͂��߁A�A�t���J��[���b�p�A���{���܂ރA�W�A�Ȃǐ��E���ɍL�����Ă��邱�Ƃ��m�F����܂����B
�@�w���v���Y�}�a�̓w���v���Y�}�Ɋ��������̌��t�����ːj��X�Ȃǂ̊O�Ȋ��A�V���~��n�G�Ȃǂ̉q�������ɂ���đ��̓ɋ@�B�I�ɓ`�d����邱�Ƃɂ���ċN����܂��B�ٔՊ������������邱�Ƃ�����Ă��܂����A�ڂ������Ƃ͂悭�������Ă��܂���B�V�����w���v���Y�}�̊�
�������ł́A��������1�T�Ԓ��x�̐������Ԃ̂̂��A�}���ɐԌ����̕\�ʂōۂ����B���ėn�����n�܂�A���t���n���Ɣ��M�A�H�~�s�U�A�ጌ���Ȃǂ̋}���Ǐ�
��܂��B���̎����̌��t�̓h���W�{���������Ŋώ@����ƁA��Ɏ������ʐ^�̂悤�ɐԌ����Ɋ��������̋ۑ̂��m�F����܂����A�}�������߂���ƌ��t���̍ې��͋}���Ɍ������Ă����܂��B�}��������������Ƃł��̑̓��ł͋ۂ��Ђ����ɐ������A���������̏�ԂƂȂ��đ��̓ւ̊������ƂȂ�܂��B���������̓́A�قƂ�ǖ��Ǐ�̏ꍇ������܂����A����x����ɐB��Q�A�ċz��������a�ւ̊��̑���A����ɁA�X�g���X�ɔ������Ƌی�
�ǂ��Ĕ����鋰�������܂��B
�@�w���v���Y�}�̓e�g���T�C�N������j���[�L�m�����n�̍R�������Ɋ��������܂����A��܂ŏǏ��}���邱�Ƃ͂ł��Ă��A�̂��犮�S�ɔr�����邱�Ƃ͌����I�ɂ͂ł��܂���B�܂��A���ʓI�ȃ��N�`�����J������Ă��Ȃ����߁A��ؓ����Ȃǂŕۋۓ��_��ɂ������܂ꂽ�ꍇ�A�_��Ƀw���v���Y�}����݂��Ă��܂��m�������ɍ����Ȃ�܂��B�������A�_��Ƀw���v���Y�}���N�������ꍇ�ł��A�����┭�Ǘ������܂荂���Ȃ����߂ɐN�����ɂ͖��炩�Ȗ�肪�F�߂��Ȃ��ꍇ�������A�������g�債�����ƂɂȂ��Ĕ���x���̔�����ɐB���т̒ቺ�ȂǂŔ_�ꐬ�тɉe�����o����A���̕a���̂Ƃ̍�����������Q�Ƃ��Č��ꂽ�肷��\��������܂��B
�@�w���v���Y�}�̐f�f�́A�}���������̋ی��ǂǂ��Ă��鎞���ł̓M���U���F�������t�h���W�{���������Ŋώ@���邱�Ƃōs���܂����A�ۂ����炩�Ɋώ@�ł�����Ԃ�
�Z�����߂Ɍ��o���x�͂��܂荂������܂���B�X�C�X�ɂ��Ă͊ԐڐԌ����ÏW������ELISA�ɂ�錟�o�@�����p����Ă��܂����A�������ɓ���ƍR�̉����}���ɒቺ����Ȃǂ̖�肪����A�u�w�I�Ȍ����@�Ƃ��Ă͐��x�ɖ�肪����܂��B�ߔN�ł�PCR���M�����̍����w���v���Y�}�̌��o�@�Ƃ��ĉ��p����Ă��܂����A�̃w���v���Y�}�̐f�f�E�E���@�Ƃ��Ă܂��m������Ă���킯�ł͂Ȃ��A�w���v���Y�}�a�͂܂��܂��������i��ł��Ȃ��a�C���ƌ����܂��B
�����̓ɂ�����w���v���Y�}�̐Z����
�@����ł́A�M�҂��s���������̗{�؏�ɂ�����w���v���Y�}�̌����ɂ��ďЉ�܂��傤�B
�@�܂������ɂ�����A�Ɋ�������w���v���Y�}�ɂ̓X�C�X�ƃp���o����2�ێ킪���݂��邱�Ƃ͐�ɏq�ׂ܂������A���̂����X�C�X�͔�r�I�a�������������߂Ɉ�`�q��͂Ȃǂ̌������������Ă��܂����B�������A�p���o���Ɋւ��Ă͏����̌����ȍ~�A���\�N�Ԃɂ킽���Č��o���ꂽ����قƂ�ǂȂ��A�����ł�1984 �N�̋{�錧�ł̔������Ō�ɁA���̑��݂͊m�F����Ă��Ȃ��������߁A�܂��p���o�����Ĕ������A����ɉu�w�����̂��߂̌��o�@�܂Ŋm������K�v������܂����i��1�A2�j�B
�@�����Ŋm������PCR �@��11 �_��Ŏ��炳��Ă���125���̓̌��t�ɂ��Ď��{���܂����B���ʂ̏ڍׂɂ��Ă͕\2�ɂ܂Ƃ߂܂��̂ŁA�����ł͂�������Ƃ��̓��e�ɂ��ďЉ�܂��傤�B�X�C�X��11 �_�ꒆ�A�킸��1 �_��݂̂Ō��o����܂������A�p���o����11 �_�ꒆ6 �_��̓��猟�o����A�����ȏ�̔_��ɐZ�����Ă��܂����B�܂��A���ꂼ��̔_����ł̗̓z�����ɂ��Č���ƁA�X�C�X�z���_��ł�12 ����6 ���Ɣ����̓��������Ă��܂����B�p���o���z���_��ł�2 �_���60 ���ȏ�̍������l�������܂������A����2 �_��Ŗ�25���A�c��2�_��ł�10���O��݂̓̂��������Ă��邱�Ƃ�������܂����B
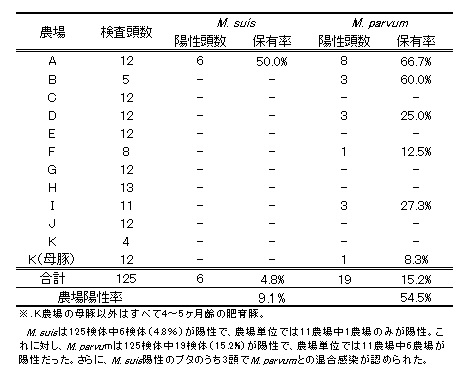
�@����ɁA�ʂ̔_��̏ɂ��Č���ƁA�X�C�X�z����A�_��͓����Ƀp���o���ɂ��Ă������z�����������A3���ɂ��ăX�C�X�ƃp���o���̍����������N�����Ă��邱�Ƃ��m�F����܂����B�܂��AK�_��ł�1���̕����p���o�������o����܂������A������͌��o����܂���ł����B
�@�����̌��ʂ͂ƂĂ������[�����e���Ǝv���܂��B�܂��A�X�C�X�ƃp���o���̔_��z�����̑傫�ȈႢ�ɂ��Ăł����A����̓w���v���Y�}�̕a�����̈Ⴂ����l����ƈӊO�Ȍ��ʂ��Ƃ����܂��B�����̊����ǂł́A�،Q���ōŏ��ɃE�C���X��ۂȂǂ̕a���̂̊��������̑̓��ŕa���̂����B���A�Q��S�̂ւƊ������L�����Ă����܂��B�X�C�X�ƃp���o�����ׂ�ƁA�X�C�X�̕a��������荂�����߂Ɋ������L����₷�����ł��B�������A�X�C�X�ƃp���o���̗������F�߂��
��A�_��ł͂ǂ���̗z�������قړ����A�ނ���p���o���̂ق�����⊴�����������Ƃ������ʂł����B����ɔ_��̉����ɂ��Ă̓p���o���̂ق������|�I�ɍ������Ƃ��m�F����܂����B���̂��Ƃ͉����Ӗ����Ă���̂ł��傤���H�@�ǂ����A�w���v���Y�}�̊�����h��̖Ɖu�Ƃ̊Ԃɂ͑��̕a���̂Ƃ͂��Ȃ������W�����藧���Ă���悤�ł��B
�w���v���Y�}�̊����Əh��̖Ɖu
�@�����ŁA���������������i��ł��鑼�̓����̃w���v���Y�}�ɂ��Ă����Ă݂܂��傤�B���Ɋ�������w���v���Y�}�ɂ̓}�C�R�v���Y�}�E�E�F�j�I�j�[�i�ȉ��u�E�F�j�I�j�[�v�j�ƃ}�C�R�v���Y�}�E�w���{�X�i�ȉ��u�w���{�X�v�j��2�ێ킪����A��ɃA�u�Ȃǂ̋z����������ē`�d����Ƃ���Ă��܂��B�k�C���ōs��ꂽ�ŋ߂̌����i��3�j�ɂ��ƁA�����������͂��ꂼ��̃w���v���Y�}�ɖ�40�����A�قړ��������Ŋ������Ă��邱�Ƃ�������܂����B�������A���n�ŕ��q����Ă���ꍇ�Ɣ_����Ŏ��炳��Ă���ꍇ�ɕ����ėz�����ɂ��Ĕ�r����ƁA�E�F�j�I�j�[�ɂ��Ă͂ǂ�����Ⴂ������܂���ł������A�w���{�X�ł͒{�ɓ��Ŏ��{����Ă����ق���3 �{���z�������������Ƃ�������܂����B���̃w���v���Y�}���z�������ɂ���ē`�d����邱�Ƃ��l����A���n�Ŏ����Ă���ق����ǂ�����������͍����Ȃ�͂��ł��B�������A�Ƃ��Ƀw���{�X�ɂ��Ă͂���܂�
�ɒm���Ă��Ȃ��������[�g�����݂��邱�Ƃ��\�z�ł��܂��B�܂��A���̂��Ƃ͂��Ƃ������w���v���Y�}�ɑ�����ۂł����Ă��A�`�d�̕��@�ɂ͈Ⴂ������Ƃ������Ƃ������Ă��܂��B
�@�܂��A�N��ʂ̊������ɂ��Č��Ă݂�ƁA�ǂ���̃w���v���Y�}��1 �` 3 �̋��ōł��z�����������A92���ȏ���̌̂������ꂩ�̃w���v���Y�}�Ɋ������A����ȏ�̔N��ɂȂ�Ə��X�ɕۗL������������Ƃ������ʂ������Ă��܂��B����͔L�Ɋ�������w���v���Y�}�ł����l�̂��Ƃ��m���Ă��āA3�Έȉ��̎Ⴂ�L�ōł��������������A10����ƌ������܂��B����͓������\���ɐ��n���A�Ɖu���l�����邱�Ƃŏ��X�ɑ̓�����w���v���Y�}���r������Ă������߂ƍl�����Ă��܂��B�w���v���Y�}�͈�x������������Ƒ̂��疝���I�Ɋ�������������Ƃ���Ă��܂������A����ł����N�ȏ�̒������Ԃ������ĉɎ���̂������Ƃ������Ƃł��B
�@���Ɍ��N��Ԃɂ��Č���ƁA�������Ă��鋍�ł͊������Ă��Ȃ����̂Ɣ�ׂĐԌ��������L�ӂɏ��Ȃ��Ƃ������ʂ�������܂����B����̓w���v���Y�}�����ɒ������Ԃ������đ̂���r������Ă����Ƃ������Ƃɂ��֘A���Ă���Ǝv���܂��B�w���v���Y�}�͐Ԍ����Ɋ��Đ������܂��B�����̖Ɖu�V�X�e���̓w���v���Y�}���̂��̂�W�I�ɂ��čU������̂ł͂Ȃ��A�w���v���Y�}�������Ԍ����𐳏�ł͂Ȃ���Ԃ��Ɣ��f���čU�����܂��B�ł�����A�w���v���Y�}���̓��ɂ������A�Ɖu�V�X�e���ɂ���ĉ��Ԍ������������܂��B���̂悤�ȐԌ����̔j�̂ɂǂ�قǂ̉e����^����̂��͒��ׂ��Ă��܂��A���t�����œ��v�w�I�ȈႢ���\��Ă���ȏ�A�ƒ{�̐��Y���ɂ��e�����o�Ă���ƍl����̂����R�Ǝv���܂��B
�@�w���v���Y�}�̔��ǂɂ͑��̕a���̂��ւ���Ă���ꍇ������܂��B�L�̃w���v���Y�}�a�͖Ɖu�͂̒ቺ�������N�����L�����a�E�C���X�iFeLV�j�ƔL�Ɖu�s�S�E�C���X�iFIV�j��ۗL���Ă���ꍇ�A���Ǘ����傫�����܂邱�Ƃ��m���Ă��܂��B�����̃E�C���X�ƃw���v���Y�}�a�̒��ڂ̊W�͖��炩�ɂ���Ă͂��܂��A���̂悤�Ȍ��ۂ͑��̓����ł��N�����Ă���̂ł͂Ȃ����Ǝv���܂��B
�{�ؐ��Y�ƃw���v���Y�}
�@���݁A�̃w���v���Y�}�a���ӎ����ė\�h�������Ă�����͂ق܂����Ȃ��Ǝv���܂����A���ƌ����ēw���v���Y�}�a���Ȃ��Ȃ��Ă���킯�ł͂���܂���B����ł́A����قǂ܂łɓ̃w���v���Y�}����莋����Ȃ��Ȃ����w�i�ɂ͉�������̂ł��傤��?�@����ɂ͗{�ؐ��Y�̋Z�p�I�Ȑi�����傫���v�������̂ł͂Ȃ����Ǝ��͎v���Ă��܂��B�V���~�Ȃǂ̉q�������̃R���g���[������̃O���[�v�����������ƁA�����čR�������̎g�p�Ȃǂ��w���v���Y�}�a�̔������N���ɂ��������̂ł͂Ȃ����Ǝv���܂��B�w���v���Y�}�̓e�g���T�C�N�����n�̍R�������Ɋ������邽�߁A���Y�����a��琬���̔x����Ȃǂł����̖�܂��g���Ă����ꍇ�A�w���v���Y�}�a�̔��ǂ�Ĕ����}�����܂��B
�@�܂��A���̗{�؏b��Âł͓̌̂�f�Â��邱�Ƃ��قƂ�ǂȂ��A���t���������Ŋώ@������A���������̑���Ńw���v���Y�}�a���E������邱�Ƃ��N����ɂ����Ȃ��Ă��邱�Ƃ�����Ǝv���܂��B
�@�������A�w���v���Y�}�����ׂĂ̔_�ꂩ��o�ł��ꂽ�Ƃ����킯�ł͂���܂���B�C�Â��Ȃ������ɖ�肪�ĔR���Ă�����A�����Ȃ��`�Ő��Y���ɉe����^�����肵�Ă��邱�Ƃ��\���l�����܂��B�ŋ߂ł̓e�g���T�C�N�����n�R�������ɑ����ܑϐ��ۂ̑������w�E����Ă��邱�Ƃ���A�ȑO�Ɣ�ׂđI�����T�����邱�Ƃ������Ǝv���܂��B���̂悤�ȏ�ʂɂ����āA����܂ŗ}�����Ă����w���v���Y�}�a�̔������Ăэ��܂邱�Ƃ��\���ɍl�����܂��B
�@���ہA���݂̐��Y����ɂ����ē̃w���v���Y�}���ǂ̂悤�Ȗ����N�����Ă���̂��͕������Ă��܂���B�������A�f�f���̂��̂��قƂ�Ǎs���Ă��Ȃ����̏ł́A�w���v���Y�}�ɂ��e����������ɂ���Ă��������̂ł͂Ȃ����Ǝ��͎v���܂��B����̃w���v���Y�}�����̔��W�Ɋ��҂��邽�߂ɂ��A�����Ŏ����\�z����w���v���Y�}�̉e���ɂ��Ă������Љ�����Ǝv���܂��B
�@���N�`���v���O�����ւ̉e��
�@�w���v���Y�}�͒��ːj�̋��p�Ŋ������L����ƍl�����Ă��邽�߁A���N�`���ڎ�ɂ�銴���̊g�傪�m���ɋN�����Ă���Ǝv���܂��B�w���v���Y�}�͊������Ă��琔���`1 �T�Ԓ��x�̐������Ԃ��o�āA�ی��ǂ��N����܂��B�ł�����A���N�`���v���O�����̑g�ݗ��ĕ��ɂ���ẮA�ŏ��̃��N�`���ڎ�Ŋ������Ĕ��ǂ������玟�̃��N�`���̃^�C�~���O�ő��̓Ɏ��X�Ɗ������L���Ă��܂����Ƃ�����Ǝv���܂��B�p���o���͖��炩�ȗՏ��Ǐ���������A�܂����ǂ����Ƃ��Ă����t���قƂ�ǎ����Ȃ����߂ɓɈُ킪����ɂ����A���N�`���̐ڎ��ɓ̒��q�������Ȃ�Ƃ��A���N�`���̌��ʂ����҂ǂ���Ɍ���Ȃ��Ƃ������`�ʼne�����Ă���ꍇ������Ǝv���܂��B
�A�ɐB���тւ̉e��
�@����L�̌����Ŏw�E���ꂽ�悤�ɁA�̃w���v���Y�}�ł��Ⴂ�̂Ńw���v���Y�}�̊������������Ȃ��Ă��邱�Ƃ����肻���ł��B�ɐB�p�X�V�ł͎g�p���郏�N�`���̎�ނ������A���̓_�ł��������X�N�͍������ł��B���Y���⏋�M�̃X�g���X�Ńw���v���Y�}�a���Ĕ����A�{���̔ɐB���т������ł��Ȃ��Ƃ��A��،Q�̖Ɖu�����肵�Ȃ��Ȃǂ̉e�������肻���ł��B�����̎������Ԃ��l����ƁA��̐��Y���ԑS�̂ł͊����̗L���ő傫�ȈႢ���o�邩������܂���B
�B���������ǂ̔��������Ƃ���
�@���̗{�؋ƊE�ɂ͂��đ��݂��Ȃ������V���������ǂ��������A����ɕ����̕a���̂̍������������ƂȂ��Ă��܂����A�Ƃ��ɁAPRRS ��PCV2 �Ƃ������̖Ɖu�ɉe����^����a�C�̔����Ƀw���v���Y�}���ւ���Ă��邱�Ƃ����Ȃ肠��̂ł͂Ȃ����Ɨ\�z����܂��B����̒����Œ��ׂ��w���v���Y�}�̐Z���ɂ��Č���ƁA�������Ӗ��̂��鐔���Ɍ����Ȃ�������܂���B�����̂͂����肵�Ȃ���������Ă���_��ł́A��x�w���v���Y�}�̐Z���ɂ��Ă����ׂĂ݂�̂�������������܂���B
�@�Ȃ��A�������������_��ł͂Ƃ��Ɏ��̗��������Ƃ��������������������ǂ̖�������Ă����킯�ł͂Ȃ��A�����w���v���Y�}�����݂��Ă��邩��Ƃ����Ē����ɉe�����o��Ƃ͌����Ďv���܂���B�������A�w���v���Y�}�̑��݂����̌����ƍ��킳���ĉe�����邱�Ƃ͍l������Ǝv���܂��B
�w���v���Y�}�̑�
�@�w���v���Y�}�̊����͒��ːj�Ȃǂ�����@�B�I�ȓ`�d����̂ƂȂ邽�߁A�����I�ɂ͉����_�ꂩ������Ȃ�����A�،Q���V�����������邱�Ƃ͂܂�����܂��A����̌��o�@���܂���ʂɍL�܂��Ă��Ȃ����߁A�w���v���Y�}��ۗL���铱����E���ł���킯�ł͂���܂���B�������A���o����y�ɍs����悤�ɂȂ�A��،Q����z����E�����Ĕ_�ꂩ��w���v���Y�}��o�ł���͔̂�r�I�e�Ղł͂Ȃ����Ǝv���܂��B
�@���Ē����̗{�؏�Ŏ��̗��̍������Ō^�̃X�C�X�����������Ⴊ���ꂽ���Ƃ�����܂����A��ɏq�ׂ��悤�ɓ̈ړ����Ȃ�����w���v���Y�}���_��Ԃœ`�d���邱�Ƃ͂܂��Ȃ��̂œ˔��I�ȗ��s�������K�v�͂���܂���B�펯�I�Ȕ_��h�u�Ɖq���Ǘ������Ă���A�w���v���Y�}���傫�Ȗ����N�������Ƃ͂Ȃ��Ǝv���܂����A�����_��̐��тŋC�ɂȂ���ł�����ꍇ��PCR���˗��ł��錟���@�ւɑ��k���Ă݂�̂������Ǝv���܂��B
�@�l�Ɋ�������w���v���Y�}�͒m���Ă��܂��A�܂�ɓ����̃w���v���Y�}���l�Ɋ��������Ⴊ����Ă��܂��B�̃w���v���Y�}���l�ɕa�C���N�����Ƃ������Ƃ͂قƂ�ǂȂ������ł����A�����̗{�؏��ƈ��̌��t��PCR�Ō�������ƍ����p�x�ŃX�C�X�����o���ꂽ�Ƃ���������܂��B�ǂ������ł̘b�Ȃ̂��͕�����܂��A���O�q���̖ʂ�����V���~��n�G�Ȃǂ̉q�������̋쏜�͓���I�ɍs���Ă������Ƃ��K�v�ł��傤�B
��1�@T wo genetic clusters in swine hemoplasma srevealed by analyses of the 16S rRNA and RNase P RNA genes. J. Vet. Med. Sci.73 (12):1657-1661, 2011
��2�@P revalence of swine hemoplasma srevealed by realtime PCR using 16S rRNA gene primers. J. Vet. Med. Sci. 74 (10):1315-1318, 2012
��3�@P revalence and risk factor analysis of bovine hemoplasma infection by direct PCR in eastern Hokkaido, Japan. J. Vet. Med. Sci. 74(9): 1171-1176, 2012